基于电催化的能量存储和转换装置的金属氧化物电催化剂近年来发展迅速,合理地评估催化剂的固有电催化活性是寻找最佳电催化剂的先决条件。我们通常将固有活性定义为比活性,即单位催化剂表面积上通过的电流。因此,对电催化剂比活性的精确评估高度依赖于催化剂表面积的可靠测量,所以确定电催化剂表面积十分重要。
一、准确测量电催化剂表面积的必要性
电解水、燃料电池等设备中重要的反应OER,ORR,HER,HOR都需要高活性的电催化剂,而建立合理的活性度量、正确评估催化剂电催化性能对寻找最佳电催化剂具有重要意义。电催化本质上是一种表面反应,其中反应物/产物的吸附/解吸仅在催化剂表面或附近区域发生,所以催化剂固有的电催化活性最常定义为比活性,即电流除以表面积。因此,催化剂表面积的准确测量决定了比活度的可靠性。
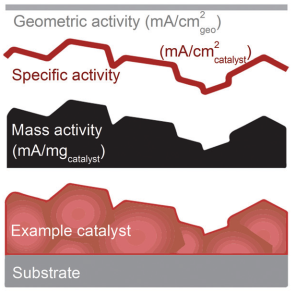
当前最常用的衡量电催化活性的四个度量是:几何活性(电流密度归一化到电极的投影几何面积mA/cmgeo2);质量活性(电流密度归一化到催化剂的负载质量);转化频率(TOF,turnover frequency,每个活性位点每秒产生/消耗的电子数);比活度(催化剂每单位实际表面积的电流mA/cmcatalyst2)。
几何活性是现在最常用的评估装置性能的实用参数,但并不反映电催化剂的固有活性,因为其未能考虑到电催化反应是表面过程,其中仅表面位点参与反应,而且几何活性常受催化剂负载量的影响,一般来说,随着负载量增加,半波电势和起始电势都会向高活性方向移动。
质量活性在很大程度上取决于电催化剂颗粒的大小(即活性位点的数量)。通过将电流密度归一化为电催化剂的负载质量来获得质量活性在锂电池等反应过程中可以作为评估不同电极材料的固有性能的合理参数,因为锂离子会深深地扩散到材料中,并且随着充电/放电而产生原裂纹[1]。但是,对于表面化学过程(例如电催化甚至超级电容器)而言,反应仅在表面/附近发生并且电极材料通常具有更好的大体积结构稳定性,所以其质量活性并不代表固有活性。质量活性的定义假设每个粒子中的所有原子都是电催化活性位,这与表面层下的内部原子不参与电催化过程这一事实相矛盾。事实是,质量活性很大程度上取决于反映表面原子分数的粒度(或等效地,催化剂的表面积)。通常,较小尺寸的催化剂表现出较高的质量活性,因为较小尺寸的颗粒具有较大的表面原子与每单位质量的总原子之比,并具有大量的电催化活性位。
TOF的确定既需要测量电流密度(将其转换为转移的电子数量),又需要对活性位点数量进行可靠的评估。电流密度可以使用电化学工作站精确测量。但是由于现代技术明确测量活性位点数量的能力有限,因此准确估算TOF仍然是一个挑战。迄今为止,获得TOF的最常用的方法是通过限定每单位表面积(例如,nm2)的表面原子数的系数将电催化剂的表面积转化为活性位点的数目。但是,该系数通常通过参考文献中的值来确定。从本质上说,直接使用文献值并不严谨,因为表面上的活性位点密度可能会随每种材料的不同而变化,每种材料可能具有不同的表面特性。另一方面,为了获得TOF,一些研究只是将催化剂的质量负载转换为活性位点的分子量。这种基于质量的TOF本质上等效于质量活动,后者假定粒子内的所有原子都是活性位点,也不能准确反映催化剂的固有活性。总而言之,TOF可以反映催化剂的内在活性,但目前很难测量。
比活性可以代表催化剂的内在活性,它是通过将电流密度归一化到电催化剂的表面积来估算比活性。由于表面积与表面原子数相关联,而表面原子数可以表示活性位点的实际数目,因此比活性实际上是每个活性位点(TOF)的活度的近似值,能够反映催化剂的固有活性。迄今为止,由于表征活性位点数量的技术能力有限,比活性是TOF的最佳替代品,被认为是研究催化剂内在活性的可靠指标。
图1. 几何活性、比活度、质量活性的示意图[2]
二、测量电化学活性面积(ECSA)的一般准则
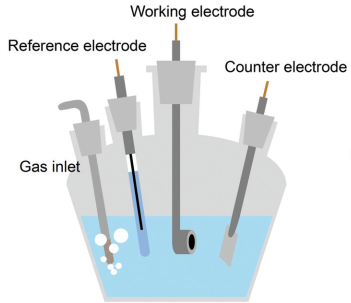
通常ECSA的测量装置选用三电极电池体系,参比电极首推可逆氢电极,饱和甘汞电极(SCE)和Ag/AgCl电极可以在酸性和中性电解质应用,而碱性条件下建议使用Hg/HgO做参比电极。电解槽的进气口是必不可少的,因为要确保测量的电流完全是由ECSA产生,而不受副反应的干扰。例如ORR,ECSA测量的电位范围通常与ORR的范围重叠,在这种情况下,电解液中的微量O2会导致ORR,干扰ECSA测量。在ECSA测量之前,应通过进气口用惰性气体(例如Ar,N2)鼓泡吹扫电解液除去溶解的氧气,在ECSA测量期间,也需要惰性气体连续鼓泡以保持电解液Ar或N2饱和。
图2. 三电极电池示意图
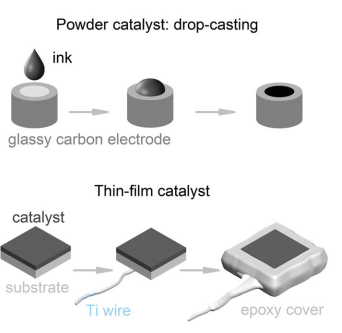
催化剂常有粉末和薄膜两种形式,样品的制备和测量其他电化学性能时样品的制备相同,在此文中就不做赘述了。有一点需要注意的是薄膜样品测量ECSA时只需要单面暴露。
图3. 粉末样和薄膜样工作电极的制备过程
三、测定金属电催化剂ECSA的技术
金属电催化剂的ECSA通常用两种方法测量:一种是测量特定表面法拉第反应的库伦电荷,例如氢的欠电势沉积(HUPD),CO汽提法,金属的欠电势沉积(UPD)和表面金属的氧化还原;另一个是非法拉第双层电容(Cdl)。
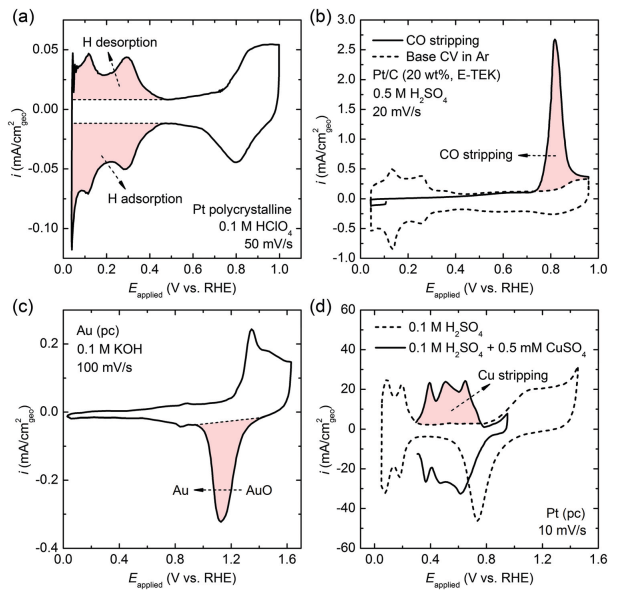
HUPD基于金属表面上氢原子的吸附和解吸。例如,在Pt表面阴极吸附单层氢原子,在阳极的解吸可以由~0.05 to ~0.4 V vs. RHE范围内的CV峰表示。减去双层电流后,对氢原子解吸和吸附区域积分。对图2a中阴影区域下的库仑电荷求平均值,然后除以比电荷(对于Pt表面的单层HUPD,比电荷为210 μC cmPt-2)[3],即可得出Pt的ECSA。HUPD已被广泛用于测定某些贵金属(例如Pt, Rh和Ir)的ECSA,尤其是用于各种电催化研究的Pt基合金。[4]
CO汽提法是通过记录在金属表面剥离一层单层CO的电荷转移来量化金属的表面积。以在Pt上的CO汽提为例,在工作电极上施加适度的还原电位,并将CO气体鼓泡到电解质中,触发Pt处的CO单层吸附。在汽提CV测量之前,需用Ar气吹扫电解液以除去溶解的CO。CO的汽提由~0.7 V vs. RHE处的氧化峰表示,并且该峰与在相同扫描速率下的基线(在Ar饱和的电解液中记录的CV)积分。为了将CO汽提的电荷转换为金属的表面积,比电荷用420 μC cmPt-2(用于在Pt形成CO单层)。与HUPD相似,CO汽提通常用于贵金属基催化剂。
对于不具有HUPD或CO汽提特征CV峰的金属,其表面积可以通过表面金属的氧化还原反应来定量,这取决于表面金属原子和氧化物种之间的相互作用。涉及一个单层金属氧化物的阳极形成,将其还原的CV峰积分并通过特定比电荷转换为表面积。例如:Ni,Ag,Cu都可以使用此种方法确定其表面积大小。
图4. Pt的HUPD和CO汽提法CV积分及计算示意图,Au, Cu通过表面金属氧化物CV峰面积确定表面积。
四、测定金属氧化物电催化剂表面积的技术
1. 基于表面氧化还原反应的测定
原则上,可以通过具有已知比电荷的金属氧化物氧化/还原的CV峰下的库仑电荷计算获得ECSA。但是与金属催化剂不同,利用金属氧化物CV峰在ECSA定量中的应用目前尚存疑问。
以电化学沉积的纳米结构Mn(III)氧化物为例,测量N2饱和的0.1 M KOH中的CV曲线,氧化峰在~0.9 V(Mn3+到Mn4 +),将氧化峰电荷积分。要将积分电荷转换为表面积,需要比电荷的值,则根据a-Mn2O3的晶格来估算比电荷的分母即面积(cmoxide2),比电荷的分子是库仑(mC),通过假设氧化反应仅穿透一个α-Mn2O3单层来计算的,其中每个Mn阳离子失去一个电子。
根据以上步骤计算金属氧化物的表面积有四点限制。首先,金属阳离子的CV峰是与单层还是多层的氧化还原反应有关尚不确定,因为氧化的渗透深度可能比一个单分子层更深,这就会影响比电荷的估算[5]。其次,同一金属氧化物的比电荷可能受合成方法,表面取向影响,例如,借助原子力显微镜确定金红石IrO2和RuO2(100)晶面上的比电荷分别为130和140 μC cmoxide-2,高于(110)晶面的表面积(IrO2为90 μC cmoxide-2和RuO2为100 μC cmoxide-2)[6]。考虑到这种差异,基于简化模型计算的比电荷或实验测得的特定材料的比电荷测量值可能并不普遍适用。第三,每个金属位点转移的电子数通常是假设确定的,这可能与实际情况有所不同。例如,假设Ni2 + / Ni3 +的特征氧化峰是一个电子转移氧化还原,则可用于量化Ni的氧化还原活性,但是,也有人发现氧化还原可能涉及正三价以外的氧化态的Ni,并且每个Ni位点的氧化还原电子转移计算高达~1.67e[7]。因此,需要准确确定金属阳离子的初始和最终氧化态。第四,对CV峰进行积分可能难以准确地计算出用于金属阳离子氧化还原的库仑电荷,其不确定性来自基线的确定,基线旨在减去背景电流。在金属催化剂上进行CO汽提或UPD时,可通过单独的测量(例如,电解液惰性气体饱和下测量CV或者缺失金属阳离子的情况下测量CV)。而金属氧化物的特征CV峰的基线基本是人为确定,这就带来了极大的误差。
2. 双电层电容法测定
双层电容(Cdl)是目前最常用的测量金属氧化物ECSA的方法,以MnO3为例,具体方法如下:在Ar饱和的0.1M KOH中,在不同扫速下记录CV曲线(10、20、50、100和200 mV s-1 电压窗口:1.1~1.2V),确保在此电压窗口中没有法拉第电流。将阳极电流或者阴极电流的平均值作为双电层电容电流ic,绘制ic相对于扫描速率v的曲线,ic遵循理想电容的理想线性行为,由ic = vCdl,则该直线的斜率即Cdl。要注意的一点是,在电催化测试中,滴涂电极时经常会添加诸如炭黑之类的导电剂以确保电导率,因此很难确定纯金属氧化物粉末的内在活性。为了使Cdl完全由氧化物贡献,用滴涂法制备电极时不应使用碳黑等导电剂,因为高表面积的碳黑会贡献非法拉第电流并干扰ECSA计算。
另一种测量Cdl的方法是电化学阻抗(EIS),通过建立等效电阻来拟合确定双电层电容值,这种方法比CV曲线的使用频率低。
3. 原子力显微镜(AFM)法测定
AFM能够以高精度可靠地评估金属氧化物的表面积,但它仅适用于具有清晰表面且表面粗糙度低的薄膜电极(例如外延生长和电沉积的薄膜电极)。薄膜电极的比活性的准确性被认为是最高的,这是因为AFM不仅排除了导电添加剂(例如炭黑)和Nafion粘合剂的影响,而且也排除了表面积测量的不确定性。
4. BET法测定
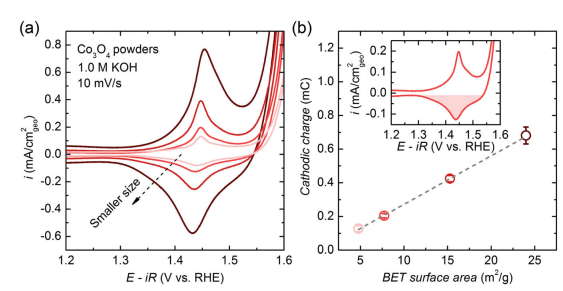
由于难以确定ECSA(如上所述),目前BET表面积是计算粉末金属氧化物催化剂比活度的最佳替代方法。BET方法利用探针气体分子(最常见的是N2,在某些情况下为CO,O2,H2等)的等温物理吸附来测量材料的比表面积。尽管BET方法可准确测量粉末材料的表面积,但我们更应该关注的是使用BET表面积计算比活性的有效性。BET表面积绝对不等于真实的ECSA,但它是真实ECSA的合理反映。有研究证明通过CV峰计算出的库仑电荷与BET表面积成线性比例(图5),这表明BET表面积能够合理地代表粉末电极的ECSA。
图5. 具有各种粒径的Co3O4尖晶石氧化物表面氧化还原反应的库仑电荷与BET表面积之间的相关性[8]
5. 电镜法测定
用透射电子显微镜或者扫描电子显微镜选取大量颗粒(通常大于200个)测量其直径(水平方向和竖直方向粒径的平均值),通过假设球形几何近似值,可根据图6中相关公式计算表面积(图6:As为比表面积,r为氧化物堆积密度),这种基于电子显微镜图像的表面积计算的误差主要源于所有粒子均为球形的假设与、不规则的真实形态之间的差异。此外,材料密度(r)通常是未知的,作为堆积密度可能会影响精度。由于球面近似和密度的不确定性,通过TEM或SEM观察计算的表面积准确性较低。
图6. 电镜法测定样品表面积

五、各类测定方法的适用性及准确性评估
表1. 金属氧化物电催化剂表面积测量的实验方法总结与比较
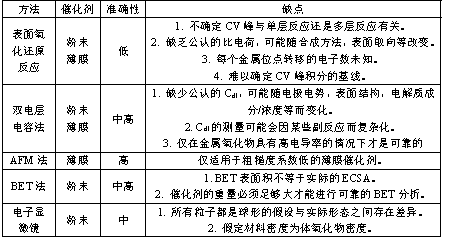
对于所有金属氧化物电催化剂(粉末或薄膜形式),如果可以克服表1所示的缺点,以ECSA方法(表面氧化还原反应或Cdl获得ECSA)作为计算比活性的首选。否则,使用非电化学方法更加合适。对于薄膜催化剂,AFM测出的表面积计算比活性更加准确。对于粉末催化剂,BET法是优选的。如果粉末催化剂的量不足以进行BET测量,则可以使用电子显微镜法估算表面积。如果粉末催化剂是复合材料,例如在碳上生长的金属氧化物颗粒,通过测量TEM图像中金属氧化物颗粒的尺寸来获得表面积较为合理。
无论是ECSA方法还是非电化学方法,都不是绝对适合表面积测量的方法,计算出实际的ECSA实际上是非常困难的。通过电化学方法估算的表面积不一定是真实的ECSA,因为ECSA测量通常不能探测电催化位点与反应中间体之间的相互作用。例如,基于Cdl的ECSA是电解质离子可及的表面积;CV峰表示与氧化物质的相互作用,但可用于自氧化/还原的位点并不等于催化的实际活性位。尽管没有完美的方法,但便捷的ECSA测量和非电化学方法仍可以用作计算比活性和揭示电催化机理的有价值的工具[9]。
参考文献:
[1] C.R. M. Winter and R. J. Brodd, 2004, 104, 4245–4270.
[2] L.C.S. J. H. Montoya, P. Chakthranont, A. Vojvodic,, N.M. T. F. Jaramillo and J. K. Nørskov, 2016, 16,, 70–81.
[3] M.M. W. Sheng, J. G. Chen and Y. Yan, Energy Environ., Sci., 6, 1509–1512.
[4] A.S.B. I. E. L. Stephens, U. Gronbjerg,, E.E.S. J. Rossmeisl and I. Chorkendorff, 2012, 6744–6762.
[5] J.A.C.S. Y. Gorlin and T. F. Jaramillo, 2010, 132,, 13612–13614.
[6] L.Q. K. A. Stoerzinger, M. D. Biegalski and Y. Shao-Horn, J. Phys. Chem. Lett., 5, 1636–1641.
[7] S.L.Y. L. Trotochaud, J. K. Ranney and S. W. Boettcher, J. Am. Chem. Soc., 136, 6744–6753.
[8] H.L.a.Z.J.X. S. Sun, Joule, 2018, 2, 1024–1027.
[9] C. Wei, S. Sun, D. Mandler, X. Wang, S.Z. Qiao, Z.J. Xu, Chemical Society Reviews, 48 (2019) 2518-2534.
本文由春春供稿。
欢迎大家到材料人宣传科技成果并对文献进行深入解读,投稿邮箱: tougao@cailiaoren.com
